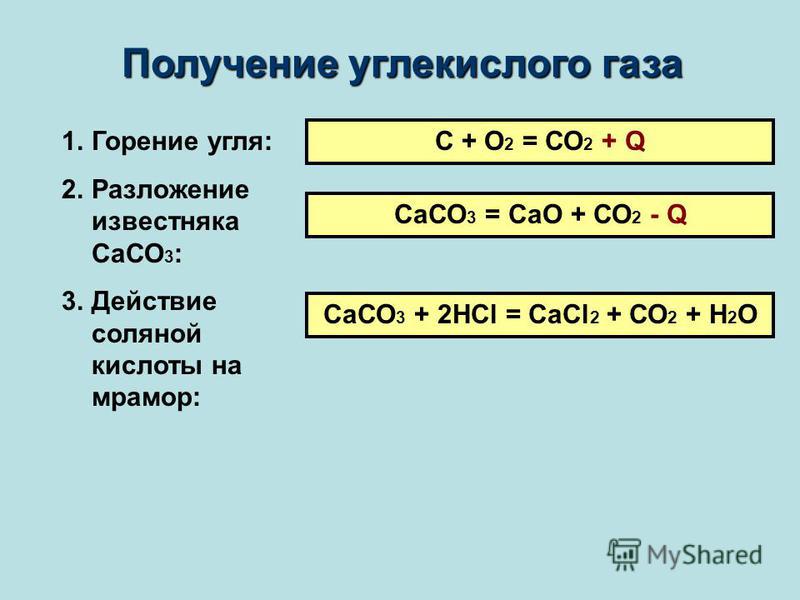
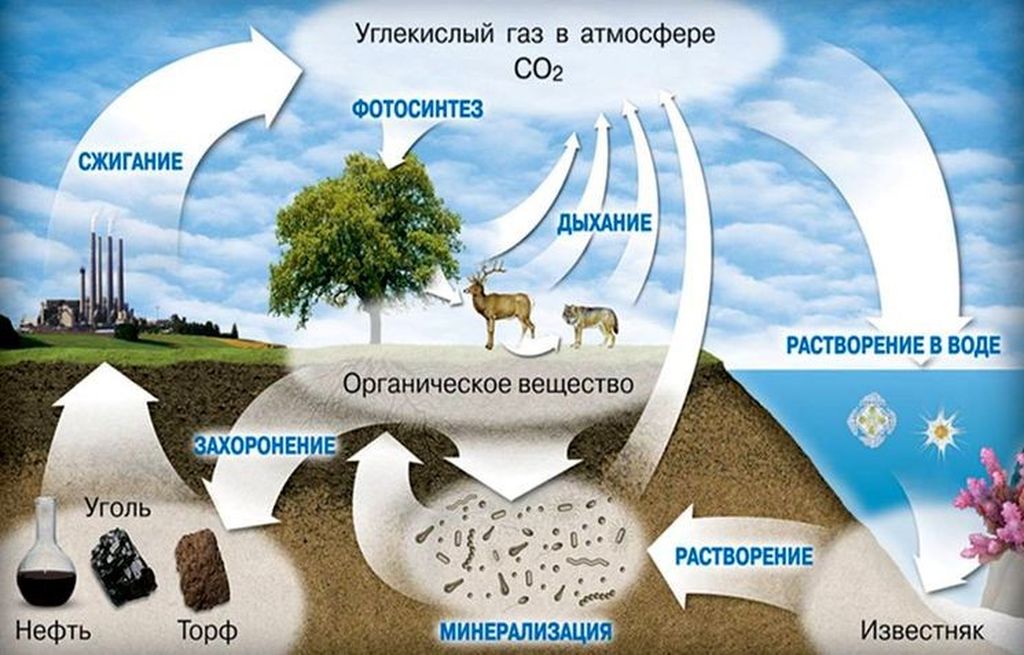
Получение углекислого газа
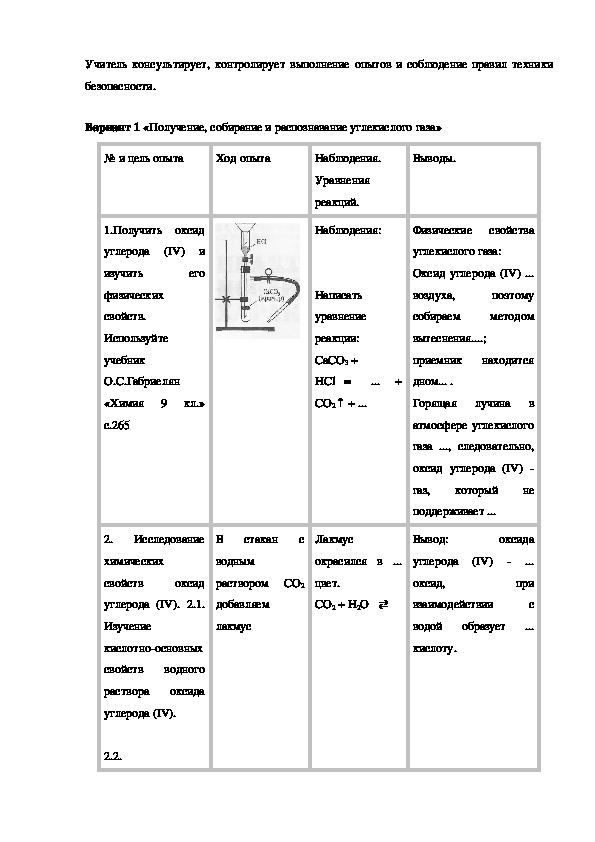
Где используется углекислый газ — сферы применения
Газовые смеси и чистые газы применяют для проведения реакций, обработки материалов и поверхностей, с их помощью получают химические соединения, которых нет в естественной среде. Разнообразные газы дают возможность получать некоторые физические явления. Широкое применение в производстве и быту находит углекислый газ. Узнайте, зачем и где применяют углекислый газ двуокись углерода , какие процессы и технологии он поддерживает в промышленности, в том числе пищевой, какими свойствами обладает, для чего нужна углекислота. Прежде чем говорить о том, где используют углекислый газ, рассмотрим, чем он является.

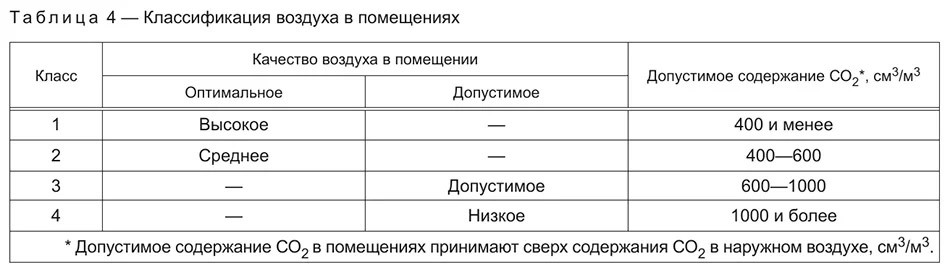
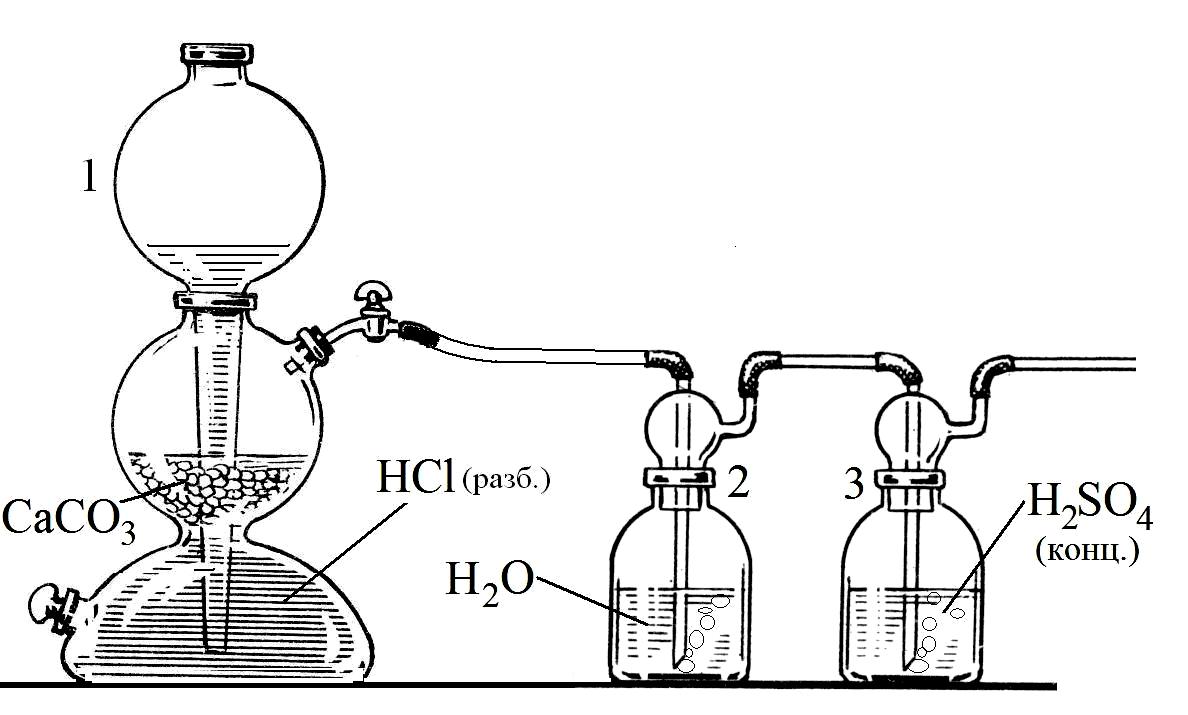









Получим углекислый газ при взаимодействии разбавленной соляной кислоты и карбоната кальция - мрамора. По трубке углекислый газ подается в стакан с известковой водой это раствор гидроксида кальция. Небольшое количество поступающего в раствор углекислого газа взаимодействует с водой с образованием слабой угольной кислоты. Углекислый газ обнаруживают по помутнению известковой воды — по осадку карбоната кальция.
- Этапы урока
- Углекислый газ двуокись углерода, диоксид углерода занимает важнейшее место среди технических газов, он широко используется практически во всех отраслях промышленности и агропромышленного комплекса. Направления использования углекислого газа в различных агрегатных состояниях многообразны — пищевая промышленность, сварочные газы и смеси, пожаротушение и т.
- Урок Химия 9 класс Базовый.
- Рубрика: Статьи о газах.
- Содержание статьи
- Получение углекислого газа и изучение его свойств практическая работа. Получим углекислый газ CO 2 при взаимодействии разбавленной соляной кислоты и карбоната кальция - мрамора.
- Опубликовано: В научной литературе диоксид углерода характеризуется, как химическое соединение, в формуле которого присутствуют следующие компоненты: 1 атом углерода и 2 атома кислорода.
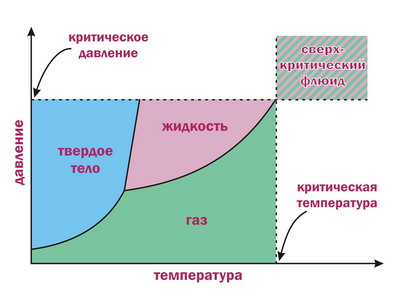
- При нормальных условиях диоксид углерода — это бесцветный газ , без вкуса и практически без запаха в больших концентрациях с кисловатым « содовым » запахом. При атмосферном давлении диоксид углерода не существует в жидком состоянии , переходя непосредственно из твёрдого состояния в газообразное возгонка.









CO2 — кислотный оксид. При этом, низшая степень окисления — 4. Благодаря этому углекислый газ проявляет окислительные свойства. Угольная кислота — одна из самых неустойчивых. В условиях атмосферного давления сразу распадается на составные соединения.